Technische und methodische Entwicklung für die hochmoderne Proteomanalyse
Im Vorfeld von massenspektrometrischen Analysen mit LC-MS/MS-Systemen für sensitive und umfassende Proteomanalysen ist die Probenvorbereitung entscheidend. Zu diesem Zwecke haben wir eine Vielzahl geeigneter Protokolle entwickelt und angepasst. Ihre Nutzung ermöglicht uns die Charaktersisierung der Proteome unterschiedlichster Mikroorganismen im Rahmen unserer eigenen Forschung oder in Zusammenarbeit mit unseren zahlreichen nationalen und internationalen Partnern.
Einige Beispiele dafür sind:
Subzelluläre Fraktionierung in Bakterien
Zur vollumfänglichen und sensitiven Charakterisierung bakterieller Proteome ist eine Fraktionierung Der Probe nach zellulärer und extrazellulärer Proteinlokalisation von Proteinen oft sinnvoll. Die Fraktionierung ermöglicht eine gezielte Anpassung der Extraktionsmethoden an die physikochemischen Eigenschaften der Zielproteine und führt zu einer umfassenderen Proteomabdeckung.
Wir haben ein effizientes Protokoll entwickelt um extrem verdünnte Proteomproben anzureichern, dass auch zur Gewinnung von extrazellulären Proteinen aus dem Wachstumsmedium genutzt werden kann. Basierend auf handelsüblichen Affinitätskügelchen erlaubt das Verfahren nicht nur die Anreicherung verdünnter Proteine, sondern auch eine sensitive Reinigung der Proben. So können beispielsweise Salze oder Nukleinsäuren entfernt werden, die anderenfalls die nachfolgenden massenspektrometrischen Analysen stören könnten. Eine weitere bemerkenswerte Eigenschaft dieses Reinigungsprotokolls ist die Möglichkeit Proteomproben ohne komplizierte Kühlungslogistik zu lagern und zu versenden.
- Bonn et al. PMID: 24987932.
- Otto et al. PMID: 28109424.
Obwohl in den meisten Mikroorganismen etwa ein Drittel des Genoms für vorhergesagte Membranproteine kodiert, bleiben diese in Proteomstudien oft unterrepräsentiert. Um das Membranproteom der Mikroorganismen zugänglich zu machen, haben wir Protokolle etabliert und (weiter)entwickelt, die sowohl Proteine der inneren und äußeren Membran als auch membranassoziierte Proteine gezielt anreichern. Diese Methoden ermöglichen eine sensitive LC-MS/MS-Analyse für verschiedene Gruppen von Membranproteinen.
- Dreisbach et al. PMID: 18491319.
- Wolff et al. PMID: 18460691.
- Maaß et al. PMID 30694509.
Auch an der Bakterienoberfläche finden sich zahlreiche Proteine mit unterschiedlichen physikochemischen Eigenschaften: Membranproteine, Lipoproteine und Proteine, die kovalent oder nicht-kovalent an die Zellwand gebunden sind. Um diese Proteine gezielt zu analysieren, haben wir spezialisierte Protokolle entwickelt; beispielsweise für die spezifische Markierung der oberflächen-assoziierten Proteine durch Biotinylierung oder den direkten proteolytischen Verdau von Oberflächenproteinen.
- Hempel et al. PMID: 20108986.
- Dreisbach et al. PMID: 21674804.
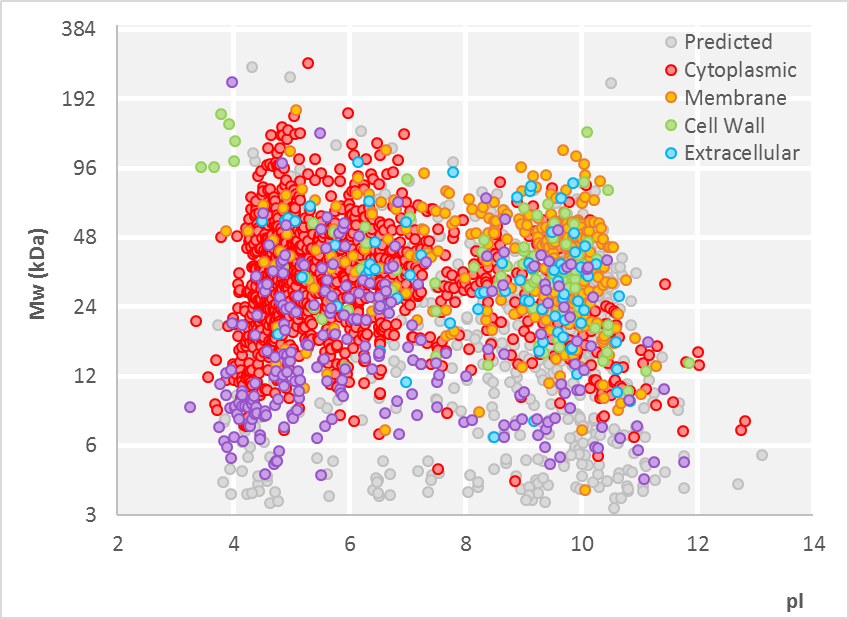
Anreicherung kleiner Proteine
Die kürzliche Entdeckung kurzer offener Leserahmen in allen Lebensformen hat es notwendig gemacht, ihre Existenz auf Proteinebene nachzuweisen und den kodierten Proteinen eine Funktion zuzuweisen. Doch kleine Proteine sind analytisch sehr herausfordernd. Sie gehen während der Probenvorbereitung oft verloren und werden bei der Ionisierung, Trennung und Detektion in der Massenspektrometrie häufig von größeren Proteinen überdeckt. Dies erschwert ihre effiziente Identifizierung und quantitative Charakterisierung. Um die Zugänglichkeit des sogenannten „Small Proteome“ zu verbessern, haben wir eine Methode zur Anreicherung dieser Proteine über Festphasenextraktion entwickelt und erfolgreich zur Kartierung des „Small Proteome“ in B. subtilis angewendet. Dabei war auffällig, dass vor allem die Detektion kleine Proteine von der Nutzung und Kombination alternativer Proteasen zu Trypsin profitieren. Unser Tool CoMPaseD hilft dabei, die leistungsstärkste Protease(kombination) für eine maximale Proteomabdeckung, nicht nur kleiner Proteine, zu identifizieren Link.
- Bartel et al. PMID: 32812434.
- Cassidy et al. PMID: 34145981.
- Bartel et al. PMID: 41541604.
Extraktion von Proteinen aus lehmhaltigen Sedimenten
Ein weiterer Schwerpunkt unserer Arbeit liegt auf der Überwindung methodischer Barrieren bei der Analyse hochkomplexer Umweltproben. Insbesondere marine Sedimente stellen aufgrund ihrer Matrixkomplexität, etwa durch hohe Tongehalte und störende Huminstoffe, eine enorme Herausforderung für die Metaproteomik dar. Diese Substanzen können Proteine binden und damit der massenspektrometrischen Analyse unzugänglich machen, was die Identifizierung mikrobieller Funktionen in den Sedimenten erschwert. Um diese Herausforderungen zu meistern, haben wir einen optimierten Extraktions-Workflow entwickelt, der eine Blockierung von Bindungsstellen durch den Einsatz von Aminosäuren mit einer hocheffizienten Elektroelution der Proteine aus dem Sedimentmaterial ermöglicht.
- Ostrizinski et al. PMID: 40568302.
Metaproteomanalysen aus Meerwasserproben
Ein zentraler Pfeiler unserer Forschung ist die Anwendung und Weiterentwicklung der Metaproteomik, um die funktionelle Dynamik mikrobieller Gemeinschaften in komplexen marinen Ökosystemen mit höchster Präzision zu verstehen. Durch die Adaptation einer effizienten Proteinextraktionsmethode, sowie den Einsatz hochsensitiver Massenspektrometrie (LC-MS/MS), sind wir heute in der Lage, nicht nur die Zusammensetzung von Bakterioplankton-Gemeinschaften zu bestimmen, sondern ihre tatsächlichen Stoffwechselleistungen nahezu in Echtzeit zu verfolgen.
- Zühlke et al. PMID: 38757353
- Beidler et al. PMID: 38744821
